فوم گرافن، راهی نوین برای تولید غضروف آزمایشگاهی در درمان آرتروز
پژوهشگران دانشگاه ایالتی بویزی (واقع در ایالت آیداهو، ایالات متحده آمریکا) با استفاده از فوم سهبعدی گرافن، روشی جدید برای تحریک سلولها و هدایت آنها به سمت تشکیل غضروف ابداع کردهاند. این تحقیق که در جلد مجله Applied Materials and Interfaces بهچاپ رسیده، امیدها را برای توسعه درمانهای مهندسی بافت در بیماری آرتروز افزایش داده است.
تحریک الکتریکی سهبعدی، راهبردی نوین در مهندسی بافت غضروف
آرتروز یا استئوآرتریت بهعنوان یکی از عوامل اصلی درد و ناتوانی حرکتی در جهان، ناشی از تخریب غیرقابلبازگشت غضروف هیالین در مفاصل است که درنهایت به درد و ناتوانی حرکتی منجر میگردد؛ بهطوریکه در موارد پیشرفته، تعویض کامل مفصل تنها گزینه درمانی موجود است. اگرچه مهندسی بافت غضروف راهحلی امیدبخش محسوب میشود، موفقیت آن در گرو شبیهسازی شرایط فیزیولوژیک طبیعی برای هدایت رفتار سلولی و تولید سازههای بافتی مشابه غضروف است اما در این مطالعه، محققان با طراحی بیوراکتورهای سهبعدی مجهز به سیستم الکتریکی، پالسهای روزانه الکتریکی را به سلولهای کشتشده روی داربستهای گرافنی اعمال کردند.
پژوهشگران در این مطالعهای جدید نشان دادند که تحریک الکتریکی مستقیم داربستهای سهبعدی گرافنی میتواند خواص مکانیکی بافت مهندسیشده را بهطور چشمگیری بهبود بخشد. این تیم تحقیقاتی با استفاده از محفظههای اختصاصی چاپ سهبعدی، پالسهای مربعی دوگانه (با دامنه ۲۰، ۴۰ و ۶۰ میلیولت در فرکانس ۱ کیلوهرتز) را به مدت ۵ دقیقه در روز و طی ۷ روز اعمال کردند.
نتایج کلیدی:
- نتایج نشان داد که تحریک الکتریکی مستقیم، رشد و خواص مکانیکی سلولهای ATDC5 (مدل شناختهشده در مهندسی بافت غضروف) را بهطور چشمگیری بهبود میبخشد. افزایش ۲۵ درصدی بهبود مدول الاستیسیته در نمونههای تحریکشده با ۶۰ میلیولت در مقایسه با گروه کنترل این موضوع را به اثبات میرساند.
- چگالی سلولی بالاتر در نمونههای تحت تحریک ۶۰ میلیولت.
- همچنین، ساختار متخلخل فوم گرافن امکان چسبندگی و یکپارچگی بهتر سلولها را فراهم کرد که گامی مهم در تولید بافتهای مهندسیشده محسوب میشود. چسبندگی و یکپارچگی بهتر سلولها در سراسر داربست گرافنی بهلطف طراحی محفظههای تحریک که غوطهوری کامل داربستهای آبگریز را در محیط کشت ممکن میسازد.
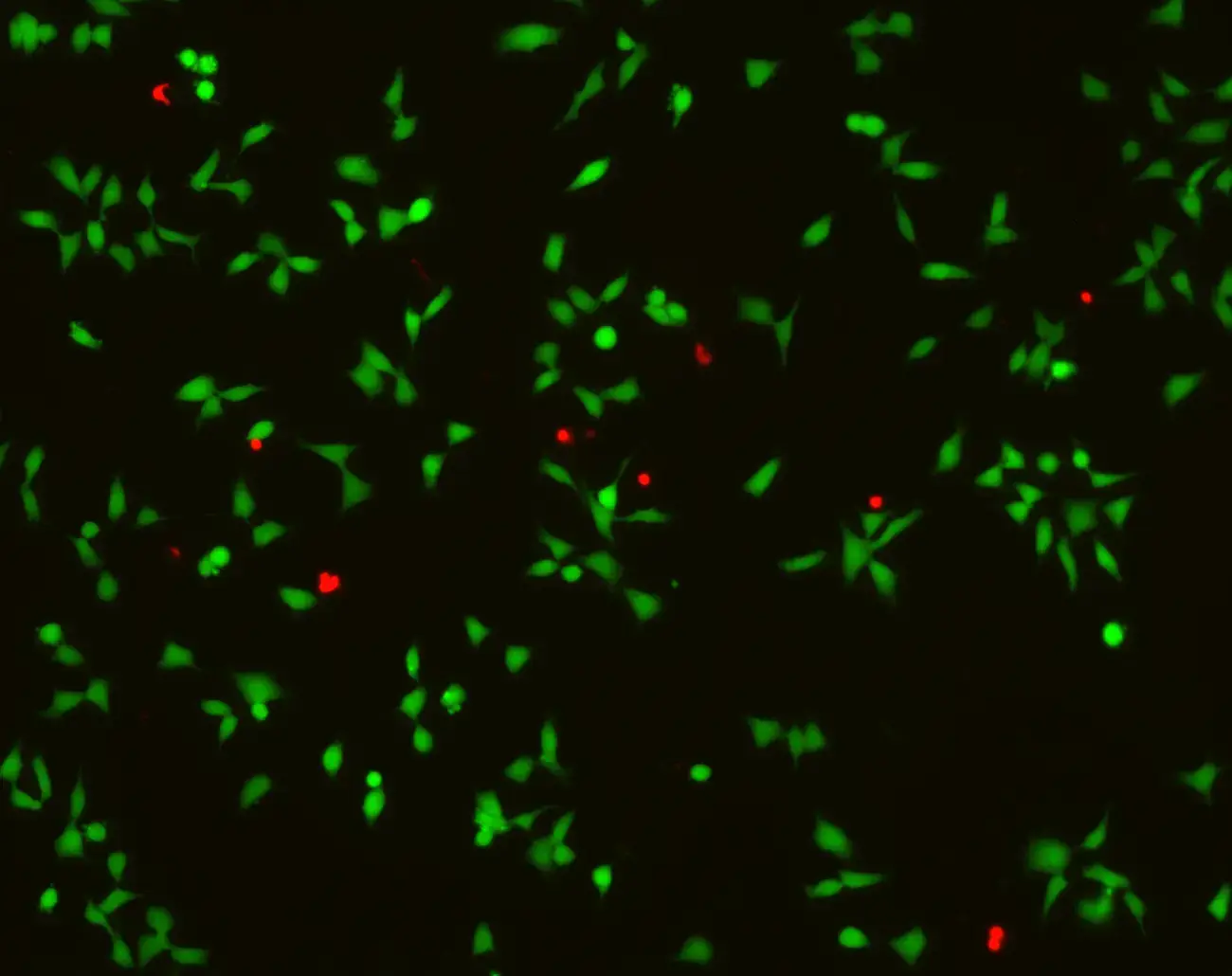
برای ارزیابی توزیع سلولی در ساختار داخلی ماتریکس داربست، محققان از میکروسکوپی کانفوکال فلورسانس و تصویربرداری میکروسیتی پرتو ایکس با کمک نانوذرات طلای کلوئیدی و رنگآمیزی فلوروفور استفاده کردند.
این یافتهها نهتنها پتانسیل تحریک الکتریکی مستقیم در بهبود خواص مکانیکی بافتهای مهندسیشده را نشان میدهد، بلکه بینشهای جدیدی درباره رفتار سلولها در داربستهای رسانای سهبعدی ارائه میکند.
مونت سویِر، نویسنده اصلی این مطالعه، توضیح میدهد:
«یکی از بزرگترین چالشها در تحریک الکتریکی سلولهای بنیادی، کنترل دقیق پارامترهای الکتریکی و تحلیل پاسخ سلولی است. سیستم ما یک پلتفرم ماژولار و مقیاسپذیر ارائه میکند که امکان تحریک الکتریکی همزمان با مانیتورینگ را فراهم میسازد.»
پروفسور دیوید استرادا نیز از دانشکده مهندسی مواد سخنان امیدوارانه را بیان میکند:
«این پژوهش درک ما از نقش سیگنالهای الکتریکی در سرنوشت سلولی و عملکرد بافت را متحول میکند و پنجرهای به سوی شناخت الکتروبیوم انسانی میگشاید.»
آرتروز با بیش از ۵۹۵ میلیون بیمار در جهان، یکی از عوامل اصلی ناتوانی جسمی است که هزینههای اقتصادی آن سالانه از ۴۶۰ میلیارد دلار فراتر میرود. تنها در آمریکا، سالانه ۶۵ میلیارد دلار صرف درمان این بیماری میشود و بیش از ۱ میلیون جراحی تعویض مفصل انجام میگیرد. این فناوری نوین میتواند در آینده به توسعه غضروف مصنوعی باکیفیت و کاهش نیاز به جراحیهای پیچیده کمک کند. همچنین این مطالعه گامی مهم در جهت توسعه روشهای درمانی کارآمد برای دیگر بیماریهای تخریب غضروف محسوب میشود.
برای مطالعه کامل خبر میتوانید از اینجا استفاده نمایید.